Como dijo en una ocasión Richard Feynman, astrofísico estadounidense ganador del Premio Nóbel y uno de los padres de la física cuántica, “Si crees que entiendes la mecánica cuántica, es que no entiendes la mecánica cuántica”. No se nos ocurre mejor forma de empezar este artículo acerca de uno de los principios más fundamentales de esta asombrosa rama de la Física.
Durante los años 20 se establecieron los pilares de la mecánica cuántica, una disciplina que estudia la naturaleza del mundo más allá del átomo. Un mundo que no funciona acorde a las leyes de la física clásica, determinadas, en gran parte, por la relatividad general de Einstein. Los físicos vieron que el mundo cuántico no seguía las reglas del juego de nuestro mundo. Las cosas eran mucho más extrañas.
En 1924, Louis de Broglie, físico francés, estableció el principio de la dualidad onda-partícula, aquel que establece que los objetos cuánticos son, al mismo tiempo, ondas y partículas. Posteriormente, Edwin Schrödinger, físico austríaco, desarrolló las ecuaciones que permiten conocer el comportamiento ondulatorio de la materia. Teníamos casi todos los ingredientes de la física cuántica.
Pero faltaba algo. Y en 1927, Werner Karl Heisenberg, físico teórico alemán, postuló el que pasó a conocerse como Principio de Incertidumbre, uno de los símbolos de la revolución de la mecánica cuántica. Un suceso que marcó un antes y un después en la historia de la ciencia al cambiar por completo nuestra visión acerca del Universo. Prepárate para que te estalle la cabeza, porque en el artículo de hoy nos sumergiremos en los misterios de la relación de indeterminación de Heisenberg.
- Te recomendamos leer: “Las 11 dimensiones del Universo (explicadas)”
¿Qué es el Principio de Incertidumbre de Heisenberg?
El Principio de Incertidumbre de Heisenberg, Principio de Indeterminación de Heisenberg o relación de indeterminación de Heisenberg es un enunciado que, a grandes rasgos, establece que, en el marco de la mecánica cuántica, es imposible medir de forma simultánea y con infinita precisión un par de magnitudes físicas.
En otras palabras, cuando estudiamos dos magnitudes conjugadas, algo que se aplica sobre todo a la posición y momento (para no complicarlo, hablaremos de ello como la velocidad) de un cuerpo, no podemos conocer los valores exactos de ambas magnitudes a la vez. El principio establece la imposibilidad de que pares de magnitudes físicas observables y complementarias sean conocidas simultáneamente y con precisión infinita
Sí, seguramente no se ha entendido nada. Pero vayamos paso a paso. El principio nos dice que cuando mejoramos la precisión en la medida de una magnitud, estamos estropeando inevitable y necesariamente la precisión de la otra magnitud. Y llega ahora el momento de hablar de posición y velocidad.
Recordemos que estamos hablando del mundo cuántico. El mundo relativista, pese a que también está sujeto a este principio de indeterminación, no contempla la influencia de este principio. Pensemos en un electrón, un tipo de fermión de la familia de los leptones con una masa unas 2.000 veces inferior a la de los protones. Una partícula subatómica que, como tal, está sujeta a las reglas del juego de la mecánica cuántica.
Y este principio de incertidumbre es la regla por excelencia. ¿Tú cómo imaginas el electrón? ¿Como una bolita? Comprensible, pero incorrecto. En la física relativista, el electrón y las otras partículas subatómicas se pueden imaginar como esferas. Pero en la cuántica, la cosa es más compleja. Son, en realidad, ondas. Ondas que van acorde a las ecuaciones de Schrödinger. Y esta indeterminación es una consecuencia de la naturaleza ondulatoria de la materia en su nivel elemental.
Imagina que quieres conocer la posición y velocidad de este electrón a la vez. Nuestro sentido común puede decirnos que esto es muy sencillo. Basta con medir ambas magnitudes. Pero en el mundo cuántico, no hay cosas sencillas. Y, de acuerdo a este principio, es totalmente imposible que, con precisión infinita, conozcas la posición y velocidad de este electrón.
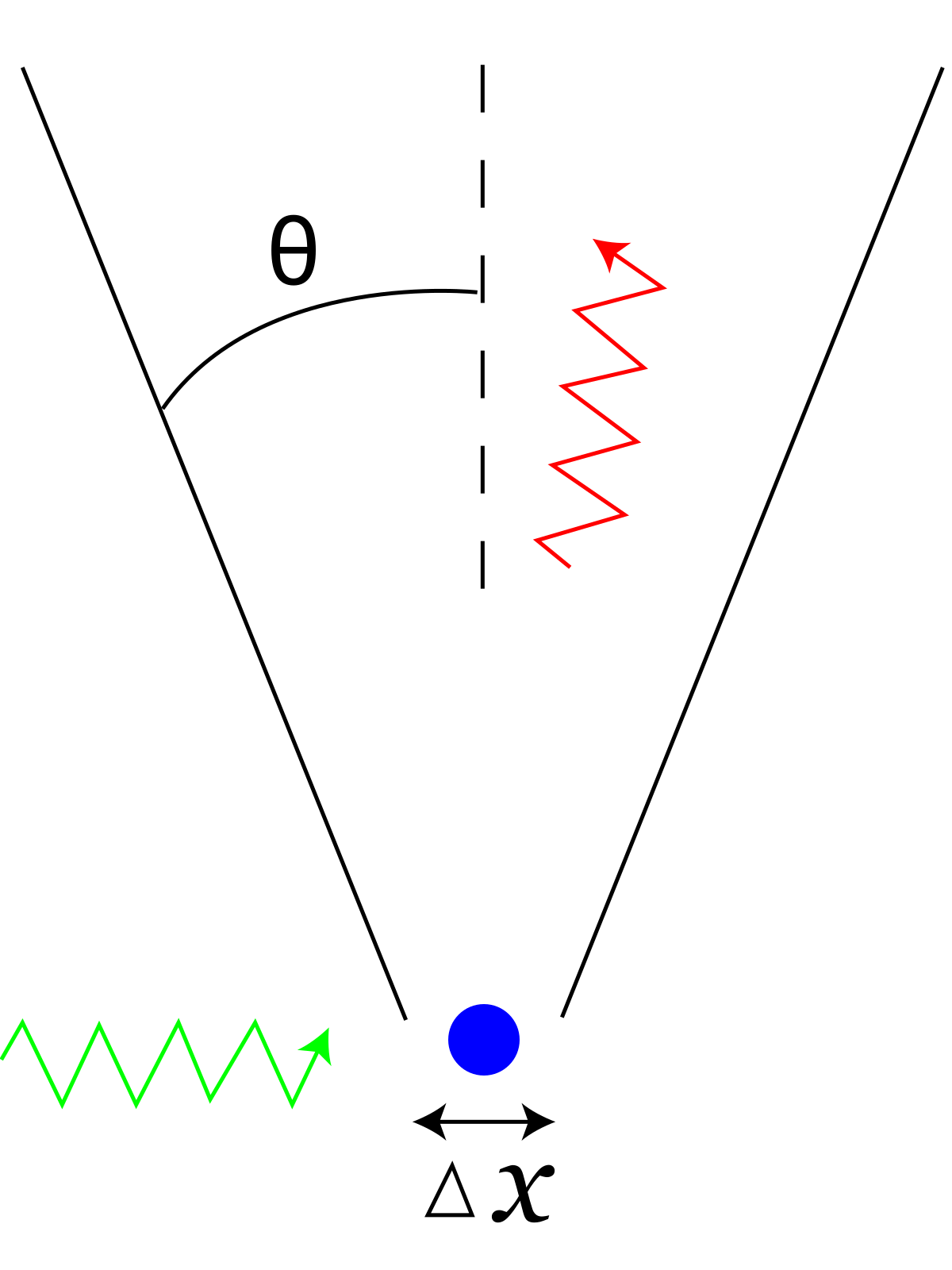
Cuando nos sumergimos en el mundo cuántico, estamos condenados a vivir en una situación de desconocimiento parcial. Por su naturaleza ondulatoria, jamás sabemos dónde está y a qué velocidad va una partícula que estamos investigando. Nos movemos en rangos. Sabemos dónde puede estar y dónde no puede estar. Sabemos a qué velocidad puede ir y a qué velocidad no puede ir. Pero es totalmente imposible que sepamos exactamente dónde está y a qué velocidad va.
Es más, si nos esforzamos en dar mucha precisión a conocer la posición de la partícula subatómica, más aumentará el rango de posibles velocidades (en lenguaje más técnico, sus momentos). Dicho de otra forma, si la incertidumbre en la medida de la velocidad fuese 0, es decir, conociéramos perfectamente su velocidad, entonces no sabríamos absolutamente nada de su posición. Podría estar en cualquier lugar del espacio.
En resumen, el Principio de Incertidumbre de Heisenberg marca un límite a la precisión con la que podemos medir pares de magnitudes conjugadas. Y aunque generalmente se use para hablar de la imposibilidad de conocer la posición y velocidad de una partícula simultáneamente, también se aplica a los pares de energía-tiempo o posición-longitud de onda, por ejemplo. Es la base de la física cuántica porque nos enseña cómo es inevitable vivir en el parcial desconocimiento cuando miramos el mundo cuántico. Por este principio, las partículas son, pero no están.
- Te recomendamos leer: “¿Qué es la Física Cuántica y cuál es su objeto de estudio?”
Las matemáticas del Principio de Indeterminación: ¿qué nos dicen las fórmulas?
Evidentemente, este principio tiene sus fundamentos en las matemáticas. Aun así, si creías que estas serían más sencillas que la explicación física, mala suerte. Y es que ni siquiera nos encontramos con una ecuación, sino con una inecuación. Una desigualdad algebraica cuya operativa, a diferencia de una ecuación, no nos da un valor, sino un rango de valores para nuestra incógnita.
La inecuación que establece el Principio de Incertidumbre de Heisenberg es la siguiente:
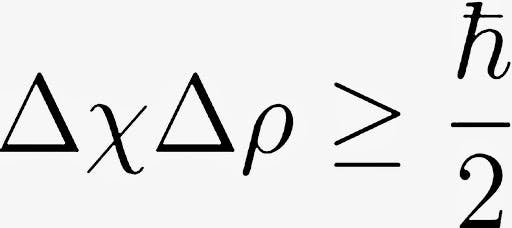
Traducido al lenguaje escrito, la inecuación expresa que la variación en la posición multiplicada por la variación en el momento (velocidad, más fácil) es mayor o igual que la mitad de la constante de Planck. Si no se ha entendido nada, tranquilidad. Tampoco es lo más importante.
Basta con entender que las pirámides de la fórmula son símbolos algebraicos que designan una variación. Es decir, un incremento o una disminución en una magnitud. Pero en el terreno de la física cuántica, estos símbolos, más que una variación, significan “indeterminación”. En otras palabras, designa que nuestra magnitud (la posición o la velocidad) se encuentra dentro de un rango. Una indeterminación alta implica que sabemos poco sobre su estado. Una indeterminación baja, que sabemos bastante.
Y es esta incertidumbre la clave de todas las medidas. Operando, podemos ver (y si no te apetece hacer números, no te preocupes, que ya te lo cuento yo) que cuanto menor es la indeterminación de una magnitud, mayor será, simplemente resolviendo la inecuación, la indeterminación en la otra. Al final, son matemáticas básicas. Es una inecuación sencilla que, eso sí, expresa una naturaleza muy compleja del mundo cuántico.
Hasta aquí, bien, ¿no? Vale. Hablemos ahora de esa extraña constante de Planck (h), una constante física clave en la mecánica cuántica. “Descubierta” por Max Planck, físico y matemático alemán, tiene un valor muy pequeño. Pequeñísimo. Para ser más exactos, h = 6.63 x 10^-34 J·s. Sí, estamos hablando de 0,0000000000000000000000000000000000663.
Y que sea un valor tan pequeño nos lleva a entender por qué este principio de incertidumbre, pese a ser una propiedad intrínseca de la materia, no se siente en nuestro mundo. Te voy a pedir que te pongas en una situación terrorífica: tu nuevo móvil se cae de la mesa. Imaginemos que yo ahora quiero determinar su posición y su velocidad concreta en un punto específico de esta caída libre en dirección al suelo.
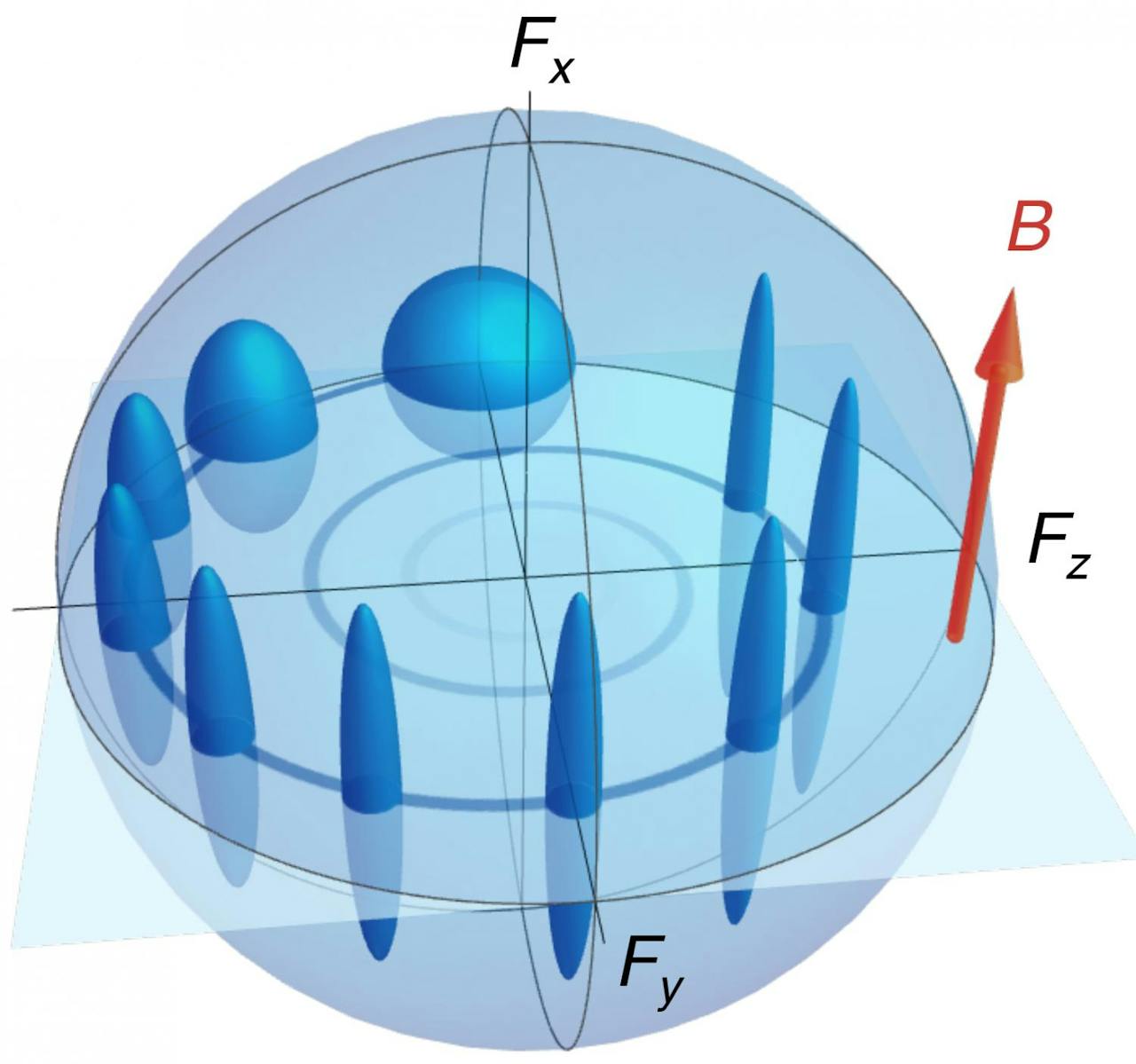
¿Puedo, con lo que has visto, saber ambas cosas a la vez? No. No puedes. El principio de incertidumbre te lo impide. “Pero yo sé exactamente dónde está el móvil y a qué velocidad va”. Sí. Puedes. Bueno, no exactamente… Lo que está pasando es que las magnitudes en las que nos encontramos (centímetros, metros, segundos…) son tan grandes en comparación con la constante de Planck que el grado de indeterminación es prácticamente nulo.
Poniéndonos un poco más técnicos, la restricción (dada por la constante de Planck) es tan increíblemente pequeña comparada con la variación de las magnitudes (a la escala de tu móvil), que esta restricción de la incertidumbre dada por la inecuación nos da igual. Por eso, en física clásica (magnitudes macroscópicas) no nos importa este principio. La indeterminación es negligible.
Ahora bien, ¿qué pasa cuando el orden de la restricción y de la variación es similar? Pues que cuidado. En la física cuántica trabajamos con unas magnitudes tan pequeñas (las partículas subatómicas son del orden de zeptómetros, es decir, la miltrillonésima parte de un metro, lo que vendría a ser 10^-21 metros. Y algunas incluso, del orden de zeptómetros, la cuatrillonésima parte de un metro, que serían 10 ^-24 metros.
¿Qué está sucediendo? Pues que las unidades de posición y de momento serán cercanas (aunque siguen siendo más grandes) al orden de la constante de Planck, que recordemos que era de 10^-34. Aquí ya sí que importa. La variación en las magnitudes es del orden de la restricción. Así que el principio de incertidumbre se expresa con mayor fuerza. Por eso la indeterminación es palpable en el mundo cuántico.
Y, recordemos, esto puedes comprobarlo tú mismo jugando con la inecuación. Verás que a escalas grandes, la indeterminación es negligible; pero a escalas subatómicas, pasa a ser importante. Y es que cuando los valores de las magnitudes son del orden de la restricción, entonces la inecuación sí que representa una restricción. Nos está restringiendo lo que podemos conocer sobre la partícula que estamos estudiando.
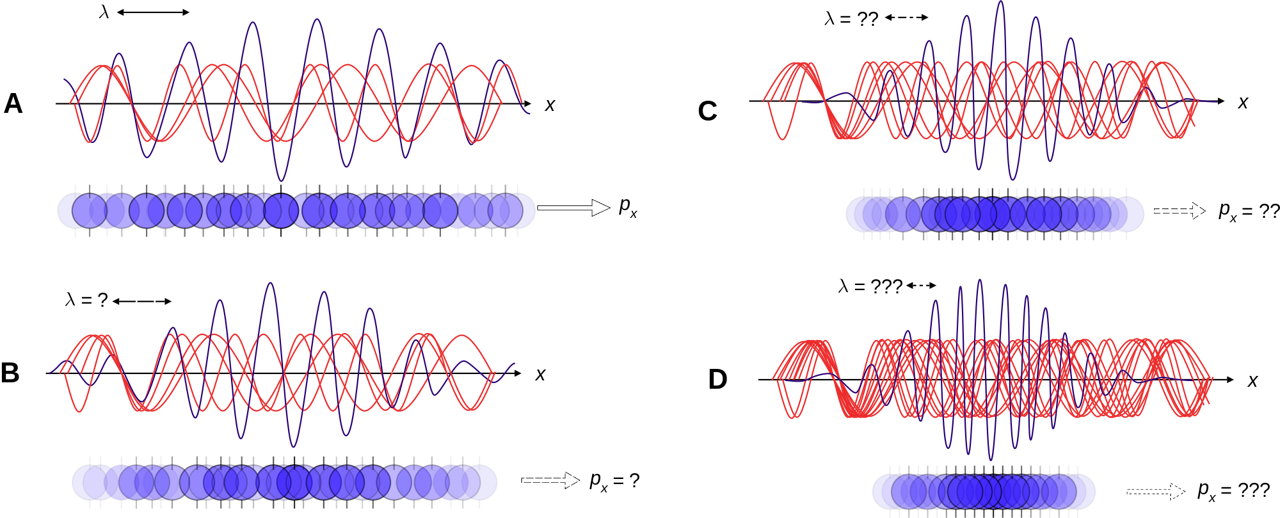
Concepciones erróneas y aplicaciones del Principio de Incertidumbre
Ha sido complicado seguro, pero has llegado al capítulo final. Y ahora es momento de hablar sobre una de las mayores confusiones dentro del mundo de la mecánica cuántica, especialmente para los menos expertos. Y esta confusión se basa en creer que el Principio de Incertidumbre está causado por nuestras dificultades para medir las partículas subatómicas o aquello que se dice de que cuando observamos algo estamos interfiriendo en su naturaleza y alterando su estado.
Y no. No tiene nada que ver. La indeterminación no se debe a la intervención experimental a la hora de medir una propiedad cuántica o a nuestros problemas para disponer de los equipos necesarios para medir con total precisión. Son cosas totalmente distintas.
Y ni siquiera con una tecnología de una civilización alienígena increíblemente avanzada podríamos medir dos magnitudes conjugadas con precisión infinita al mismo tiempo. Como hemos recalcado, el principio de incertidumbre es una consecuencia de la naturaleza ondulatoria de la materia. El Universo, por ser como es a nivel cuántico, hace que sea imposible determinar pares de magnitudes al mismo tiempo.
No es culpa nuestra. No surge de nuestra incapacidad para medir bien las cosas o porque perturbemos el mundo cuántico con nuestros experimentos. Es culpa del propio mundo cuántico. Por ello, sería mejor utilizar el concepto de “indeterminación” que el de “incertidumbre”. Cuando más determinas una cosa, más indeterminas la otra. Esta es la clave de la mecánica cuántica.
Establecer el Principio de Indeterminación de Heisenberg marcó un antes y un después ya que cambiaba por completo nuestra concepción del Universo y, además, con el tiempo nos dimos cuenta de que era uno de los principios cuánticos con mayores implicaciones en el mundo de la física, la mecánica cuántica y la astronomía.
De hecho, esta indeterminación de la materia fue una de las claves para desarrollar principios como el del efecto túnel, otro principio de la física cuántica que se desprende de esta naturaleza probabilística del mundo cuántico y que consiste en un fenómeno en el que una partícula es capaz de penetrar una barrera de impedancia mayor que la energía cinética de dicha partícula. En otras palabras y entre muchísimas comillas: las partículas subatómicas pueden atravesar paredes.
Del mismo modo, la radiación de Hawking (una teórica radiación emitida por los agujeros negros que haría que lentamente se evaporaran), la teoría de la inexistencia del vacío absoluto (no puede existir el espació vacío), la idea de que es imposible que se llege al cero absoluto de temperatura y la teoría de la energía del punto 0 (que impone una energía mínima en el espacio que permite la creación espontánea de materia en lugares donde aparentemente no hay nada, rompiendo, durante un instante, el principio de conservación) nacen de este principio.
Después de tantos intentos por determinar la naturaleza de todo aquello que nos compone y que nos rodea, quizás debamos aceptar que, en su mundo más elemental, el Universo es indeterminado. Y cuanto más luchemos por determinar algo, más indeterminaremos otra cosa. El mundo cuántico no entiende de lógica. No podemos pretender que lo haga.

















