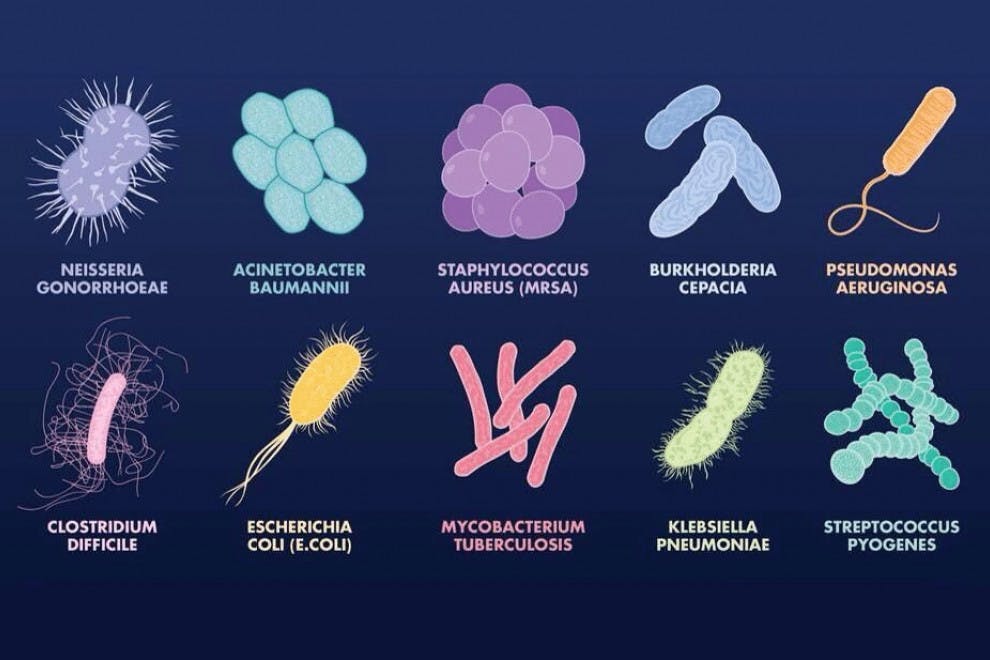
Todo en la naturaleza es, básicamente, pura química. Desde los procesos para obtener bebidas alcohólicas hasta la replicación de nuestro ADN para que nuestras células se puedan dividir, la vida tal y como la conocemos se basa en reacciones bioquímicas.
Las rutas metabólicas son procesos químicos de conversión de moléculas. Es decir, partiendo de un metabolito inicial, este sufre transformaciones hasta convertirse en un metabolito final importante para la fisiología de algún ser vivo.
Pero, ¿cómo ocurren estas transformaciones? ¿Cuál es la fuerza que las impulsa? Bueno, evidentemente, no suceden por arte de magia. Y, en este sentido, entran en juego las enzimas, que son unas moléculas intracelulares que inician y dirigen estas rutas metabólicas.
Solo en el cuerpo humano existen unas 75.000 diferentes (y hay otras presentes en otros seres vivos que nosotros no tenemos), aunque, dependiendo de en qué basan su acción metabólica y cuál es su finalidad, estas pueden clasificarse en 6 grupos principales. Y en el artículo de hoy analizaremos las características de cada uno de ellos y veremos las funciones y ejemplos.
- Te recomendamos leer: “Las 30 principales enzimas celulares (y sus funciones)”
¿Qué son las enzimas?
Las enzimas son, hablando metafóricamente, los directores de orquestra de nuestras células (y de las de los otros seres vivos), pues se encargan de ordenar, dirigir y estimular a todos los otros componentes celulares para que desarrollen su parte en la “obra”.
Y, hablando biológicamente, las enzimas son moléculas intracelulares que activan cualquier ruta metabólica de la fisiología de un organismo. Es decir, todas aquellas reacciones bioquímicas para que la célula (y el conjunto de células) se mantenga viva, obtenga energía, crezca, se divida y se comunique con el entorno son posibles gracias a estas moléculas activadoras.
En este sentido, las enzimas son proteínas que actúan como catalizadores biológicos, cosa que significa, básicamente, que aceleran (para que sucedan rápidamente) y dirigen (para que sucedan en el orden correcto) todas aquellas reacciones de conversión de un metabolito a otro, que es en lo que se basa el metabolismo.
Sin estas enzimas, las reacciones metabólicas serían demasiado lentas (y algunas ni siquiera podrían existir) y/o no ocurrirían en el orden adecuado. Intentar que alguna reacción metabólica suceda sin acción de la enzima que la controla sería como intentar prender un petardo sin encender su mecha con un mechero. En este sentido, el mechero sería la enzima.
De ahí que dijéramos que las enzimas son como los directores de orquestra de nuestras células, pues estas moléculas, que están presentes en el citoplasma celular (se sintetizan cuando su presencia es necesaria) llaman a los metabolitos que tienen que interactuar (elige a sus músicos) y, dependiendo de lo que digan los genes de la célula, encenderá un seguido de reacciones u otro (como si fuera una partitura) y, a partir de ahí, dirigirán todas las transformaciones químicas (como si de una pieza musical se tratara) hasta que se obtenga el resultado final.
Este resultado final dependerá de la enzima y de los sustratos (los primeros metabolitos de la reacción bioquímica) y puede ir desde digerir grasas en el intestino delgado hasta producir melanina (pigmento para proteger de la radiación solar), pasando por digerir la lactosa, desenrollar la doble cadena de DNA, replicar el material genético, realizar la fermentación alcohólica (estas enzimas solo existen en levaduras), producir ácido clorhídrico para el estómago, etc.
En resumen, las enzimas son proteínas intracelulares presentes en absolutamente todos los seres vivos (algunas son comunes a todos y otras son más exclusivas) que inician, dirigen y aceleran todas las reacciones metabólicas de la fisiología de un organismo.
- Te recomendamos leer: “Los 3 tipos de rutas metabólicas (y ejemplos)”
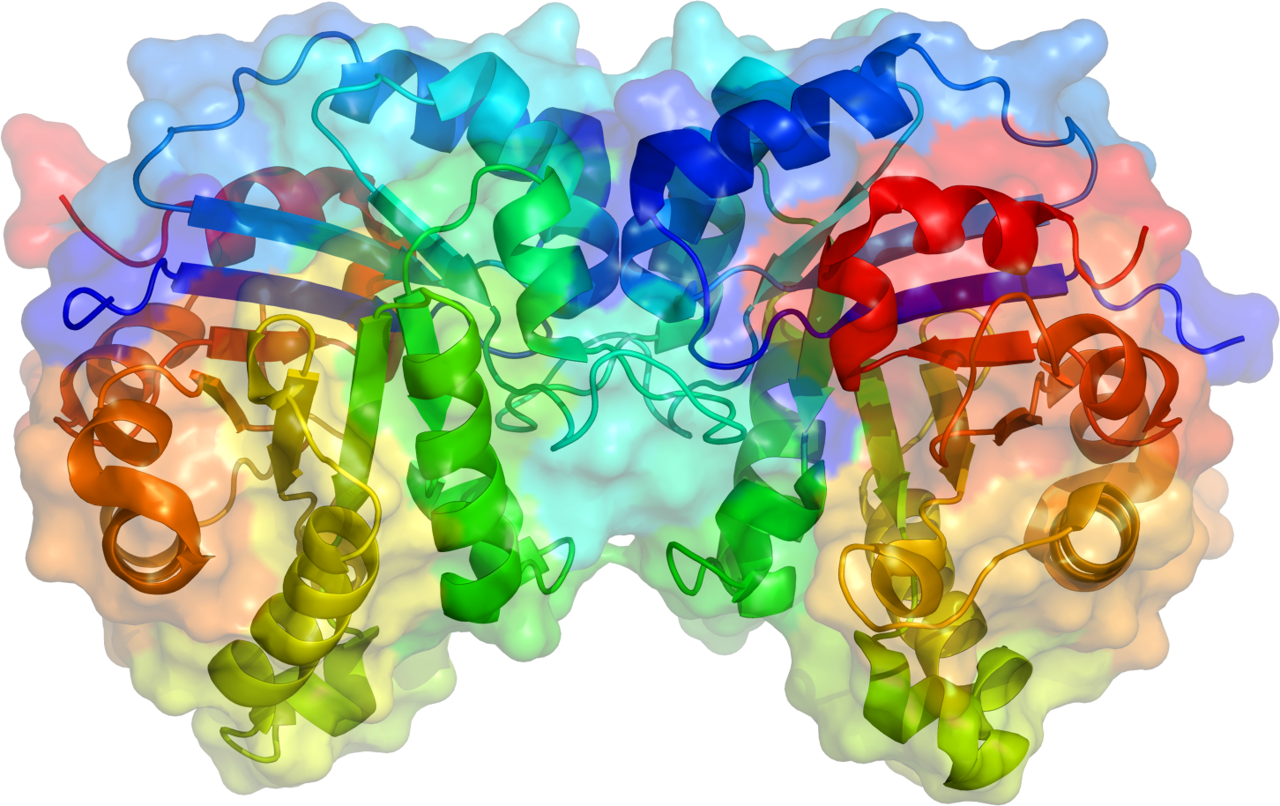
¿Cómo funcionan las enzimas?
Antes de entrar de lleno en la clasificación, es importante repasar, de forma muy breve y sintética (el mundo del metabolismo celular está entre lo más complicado de la biología), cómo funcionan las enzimas y cómo desarrollan sus acciones metabólicas.
Como hemos dicho, una enzima es una proteína, lo que significa que es, en esencia, una sucesión de aminoácidos. Existen 20 aminoácidos distintos y estos pueden unirse con combinaciones increíblemente variadas para dar lugar a “cadenas”. En función de cómo sea la serie de aminoácidos, la enzima adquirirá una estructura tridimensional concreta, cosa que, junto con la clase de aminoácidos que contenga, determinará a qué metabolitos puede unirse.
En este sentido, las enzimas disponen de lo que se conoce como zona de unión, una región de unos pocos aminoácidos con afinidad por una molécula concreta, que es el sustrato de la reacción bioquímica que estimula. Cada enzima tiene una zona de unión diferente, por lo que cada una atraerá a un sustrato (o metabolito inicial) concreto.
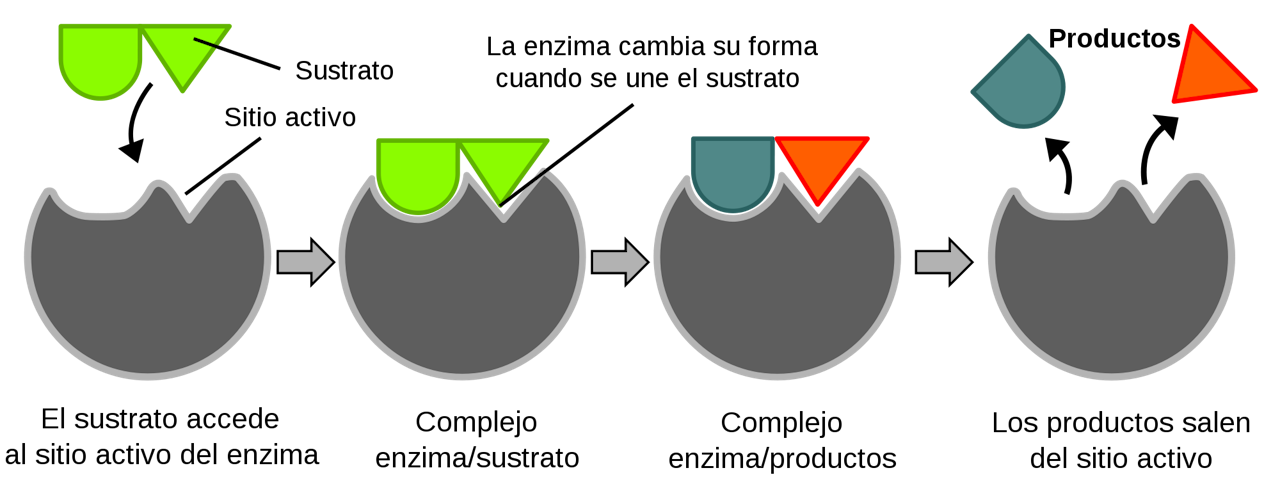
Una vez el sustrato se ha enganchado a la zona de unión, como este está incluido dentro de una región mayor conocida como sitio activo, empiezan a estimularse las transformaciones químicas. En primer lugar, la enzima modifica su estructura tridimensional para englobar perfectamente el sustrato en su interior, formando lo que se conoce como complejo enzima/sustrato.
Una vez se ha formado, la enzima realiza su acción catalítica (después veremos cuáles pueden ser) y, consecuentemente, las propiedades químicas del metabolito que se ha unido cambian. Cuando la molécula obtenida es diferente a la inicial (el sustrato), se dice que se ha formado el complejo enzima/productos.
Estos productos, a pesar de que proceden de una transformación química del sustrato, ya no tienen las mismas propiedades que este, por lo que no tienen la misma afinidad por la zona de unión de la enzima. Esto provoca que los productos salgan de la enzima, listos para realizar su función en la fisiología de la célula o preparados para funcionar como sustrato de otra enzima.
¿Cómo se clasifican las enzimas?
Habiendo entendido qué son y cómo funcionan a nivel bioquímico, podemos pasar ya a analizar los distintos tipos de enzimas que existen. Como hemos dicho, existen más de 75.000 enzimas diferentes y cada una de ellas es única, pues tiene afinidad por un sustrato concreto y, consecuentemente, realiza una función específica.
De todos modos, la Bioquímica ha sido capaz de realizar una clasificación de las enzimas dependiendo de las reacciones químicas generales que estimulan, dando lugar así a 6 grupos donde cualquiera de las 75.000 enzimas existentes puede entrar. Veámoslos.
1. Oxidorreductasas
Las oxidorreductasas son enzimas que estimulan las reacciones de oxidación y reducción, conocidas “popularmente” como reacciones redox. En este sentido, las oxidorreductasas son proteínas que, en una reacción química, permiten la transferencia de electrones o de hidrógeno de un sustrato a otro.
Pero, ¿qué es una reacción redox? Una reacción de oxidación y reducción es una transformación química en la que un agente oxidante y un agente reductor se alteran mutuamente su composición química. Y es que un agente oxidante es una molécula con la capacidad de sustraer electrones a otra sustancia química conocida como agente reductor.
En este sentido, las oxidorreductasas son enzimas que estimulan este “robo” de electrones, pues el agente oxidante es, en esencia, un ladrón de electrones. Sea como sea, el resultado de estas reacciones bioquímicas es la obtención de aniones (moléculas cargadas negativamente ya que han absorbido más electrones) y de cationes (moléculas cargadas positivamente ya que han perdido electrones).
La oxidación del metal es un ejemplo de reacción de oxidación (que se puede extrapolar a lo que sucede en nuestras células con distintas moléculas), pues el oxígeno es un potente agente oxidante que roba los electrones del metal. Y el color marrón resultado de la oxidación se debe a esta pérdida de electrones.
- Para saber más: “Potencial redox: definición, características y aplicaciones”
2. Hidrolasas
Las hidrolasas son enzimas que, a grandes rasgos, tienen la función de romper enlaces entre moléculas mediante un proceso de hidrólisis en el cual, como podemos deducir por su nombre, está involucrada el agua.
En este sentido, partimos de una unión de dos moléculas (A y B). La hidrolasa, en presencia de agua, es capaz de romper esta unión y obtener las dos moléculas por separado: una se queda con un átomo de hidrógeno y la otra con un grupo hidroxilo (OH).
Estas enzimas son imprescindibles en el metabolismo, pues permiten la degradación de moléculas complejas en otras de más sencilla asimilables para nuestras células. Existen muchos ejemplos. Para enumerar algunos nos quedamos con las lactasas (rompen los enlaces de la lactosa para dar lugar a glucosa y galactosa), las lipasas (degradan los lípidos complejos en grasas más simples), las nucleotidasas (degradan los nucleótidos de los ácidos nucleicos), las peptidasas (degradan las proteínas en aminoácidos), etc.
3. Transferasas
Las transferasas son enzimas que, como su propio nombre indica, estimulan la transferencia de grupos químicos entre moléculas. Son distintas a las oxidorreductasas en el sentido que estas transfieren cualquier grupo químico excepto el hidrógeno. Un ejemplo son los grupos fosfato.
Y a diferencia de las hidrolasas, las transferasas no forman parte del metabolismo catabólico (degradación de moléculas complejas para conseguir simples), sino del anabólico, que consiste en gastar energía para sintetizar, a partir de moléculas simples, moléculas más complejas.
En este sentido, las rutas anabólicas, como por ejemplo el ciclo de Krebs, disponen de muchas transferasas distintas.
4. Ligasas
Las ligasas son enzimas que estimulan la formación de enlaces covalentes entre moléculas, los cuales son el “pegamento” más fuerte de la biología. Estos enlaces covalentes se establecen entre dos átomos, los cuales, al unirse, pasan a compartir electrones.
Esto hace que sean uniones muy resistentes y especialmente importantes, en el ámbito celular, para establecer las uniones entre los nucleótidos. Estos nucleótidos son cada una de las piezas que conforman nuestro ADN. De hecho, el material genético es “simplemente” una sucesión de moléculas de este tipo.
En este sentido, una de las ligasas más conocidas es la DNA ligasa, una enzima que establece los enlaces fosfodiéster (un tipo de enlace covalente) entre los distintos nucleótidos, impidiendo que haya roturas en la cadena de ADN, cosa que tendría consecuencias catastróficas para la célula.
- Te recomendamos leer: “Las 3 diferencias entre el ADN y el ARN, explicadas”
5. Liasas
Las liasas son enzimas muy similares a las hidrolasas en el sentido que su función es la de romper enlaces químicos entre moléculas y que, por lo tanto, son pieza fundamental de las reacciones catabólicas, pero en este caso, las liasas no requieren de la presencia de agua.
Además, no solo son capaces de romper enlaces, sino de formarlos. En este sentido, las liasas son enzimas que permiten estimular reacciones químicas reversibles, por lo que de un sustrato complejo se puede pasar a uno más simple rompiendo sus enlaces, pero también se puede pasar de este sustrato sencillo a otra vez el complejo volviendo a establecer su unión.
6. Isomerasas
Las isomerasas son unas enzimas que ni rompen enlaces ni los forman y que tampoco estimulan la transferencia de grupos químicos entre moléculas. En este sentido, las isomerasas son proteínas cuya acción metabólica se basa en alterar la estructura química de un sustrato.
Cambiando su forma (sin añadir grupos químicos ni modificando sus enlaces), se puede conseguir que una misma molécula desempeñe una función totalmente distinta. Por lo tanto, las isomerasas son enzimas que estimulan la obtención de isómeros, es decir, nuevas conformaciones estructurales de una molécula que, gracias a esta modificación de su estructura tridimensional, se comportan de forma diferente.
Un ejemplo de isomerasa es la mutasa, una enzima que está implicada en la octava etapa de la glicólisis, una ruta metabólica cuya función es la de obtener energía a partir de la degradación de la glucosa.