Hay unas 500 especies de patógenos capaces de hacernos enfermar. De estas, algunas son más simples y otras más complejas a nivel anatómico, genético, fisiológico o estructural. A grandes rasgos, las bacterias y los hongos son los gérmenes más complejos, pues desarrollan funciones biológicas más elaboradas para infectarnos.
Por ello, lo normal ahora sería pensar que los virus son los más simples, pues hemos escuchado infinidad de veces que son tan sencillos que ni siquiera pueden considerarse seres vivos. Pero, ¿realmente son los más simples? No.
- Te recomendamos leer: “¿Es un virus un ser vivo? La ciencia nos da la respuesta”
En la naturaleza hay otro tipo de gérmenes mucho más sencillos a nivel biológico: los priones. Estas estructuras orgánicas son tan simples que ya no solo es que no haya ningún debate al afirmar que no son seres vivos (en el caso de los virus todavía hay división de opiniones), sino que no es más que una proteína con la capacidad de infectarnos.
En el artículo de hoy hablaremos de la naturaleza de estas increíbles estructuras que, a pesar de ser tan simples, tienen el “honor” de provocar la única enfermedad con un 100% de letalidad en el mundo. No hay ni una sola otra patología en la que la muerte, pase lo que pase, sea segura.
¿Qué es un prión?
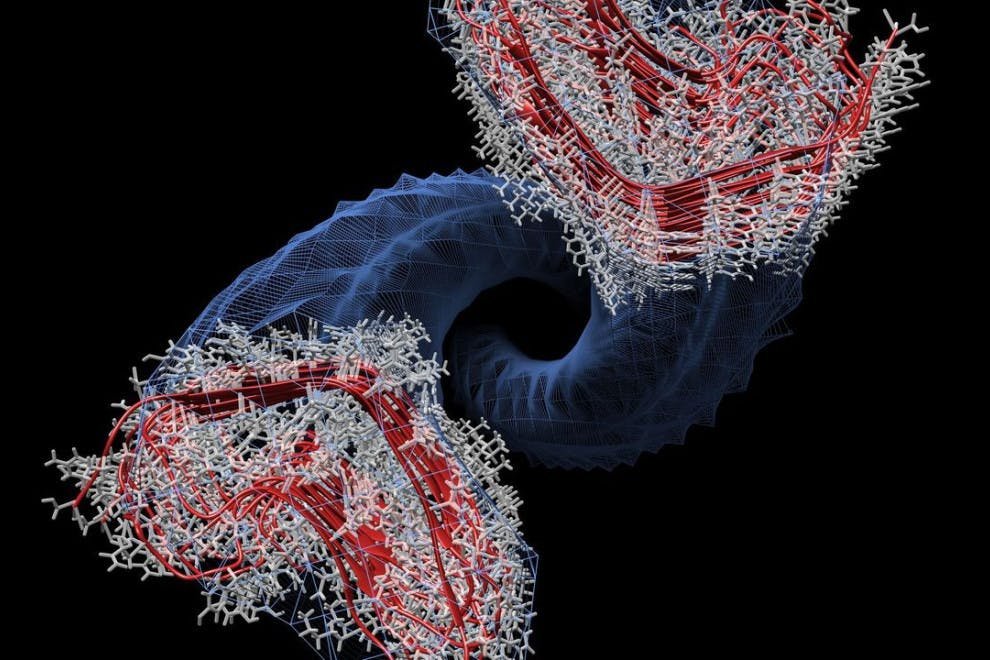
Un prión es el tipo de patógeno más sencillo de la naturaleza. Y es que es tan simple que ni siquiera tiene material genético (incluso los virus lo tienen), es decir, es capaz de desarrollar un proceso infectivo sin disponer de ningún gen que le ayude en ello. En este sentido, un prión es simplemente una proteína capaz de dañar el organismo de un individuo sano.
Estas proteínas son formas defectuosas de proteínas “sanas” de nuestro cuerpo que no cumplen con su función y que, además, tienen la capacidad de transformar a las otras proteínas en defectuosas, expandiendo así el daño por todo el sistema nervioso central.
- Te recomendamos leer: “Los 6 diferentes tipos de agentes patógenos (y sus características)”
Y es que estos priones afectan a nivel del cerebro, haciendo que las proteínas que lo conforman pierdan lentamente su estructura y función, causando así una neurodegeneración que termina provocando prácticamente siempre la muerte.
Los priones provocan las enfermedades conocidas como encefalopatías espongiformes ya que cuando se realiza una autopsia de alguien que ha muerto a causa de un prión, el cerebro se observa con agujeros, como si fuera una esponja. Los priones son patógenos raros pero que provocan enfermedades intratables y mortales.
Los priones son proteínas “zombi”
Venimos diciendo que un prión es una proteína. Pero, ¿cómo es esta proteína? Por hacer una metáfora y que después sea fácil de entender, vamos a imaginar a este prión como una proteína normal de nuestro cuerpo que se ha convertido en una “proteína zombi”. Y ahora vamos a entenderlo.
Como ya sabemos, nuestro genoma es un conjunto de genes, es decir, segmentos de DNA que serán leídos por distintas moléculas para dar lugar a proteínas. Absolutamente todas nuestras funciones biológicas y el desarrollo de nuestro organismo se basan en conseguir esta conversión de genes en proteínas.
Y estas proteínas, que son un tipo de moléculas que, por lo que acabamos de ver, están implicadas en todos los procesos del organismo, son una sucesión de aminoácidos. En esencia, una proteína sería un “collar” de aminoácidos. Pero, ¿solo importa qué aminoácidos haya? No. Y aquí es donde vamos llegando al tema que nos interesa.
Que una proteína pueda desarrollar su función depende no solo de la sucesión de aminoácidos, sino de cómo se estructura esta proteína en el espacio, es decir, qué forma coge. Cuando hay problemas en los aminoácidos o en la estructura tridimensional, la proteína pierde su función.
En nuestro genoma tenemos un gen que transcribe para una proteína determinada, la PrPc (proteína priónica celular), la cual es imprescindible para mantener un correcto equilibrio de neurotransmisores en el sistema nervioso central. Hasta aquí, todo bien.
Pero ahora es cuando entran en juego los priones. Los priones son una forma “zombi” de esta proteína. Y decimos “zombi” porque, por un lado, es la proteína defectuosa (que ha perdido su función) y, por otro lado, es capaz de transformar a las proteínas de su alrededor en otros zombis.
Cuando este prión (conocido como PrPSc), que, como hemos hemos dicho, es una proteína normal de nuestro organismo con una alteración en su estructura, llega al cuerpo por distintas vías (la más conocida es comiendo tejidos de animales enfermos con este prión, pero no es la más frecuente, como veremos), hace que las proteínas normales (las PrPc) se transformen en priones. Y cada uno de estos nuevos priones, continúa infectando a los demás, como si de una pandemia zombi se tratara.
- Te recomendamos leer: “¿Podrían existir los zombies? La ciencia nos da la respuesta”
Por lo tanto, el prión responsable de la infección está haciendo que en nuestro sistema nervioso central todas las proteínas priónicas celulares (recordemos que estas eran las proteínas sanas) se conviertan en priones. Es decir, lentamente, las proteínas sanas se están convirtiendo en defectuosas.
Pero, ¿en qué sentido las cambia? ¿Alterando su sucesión de aminoácidos? No. Eso sería demasiado complejo. Los priones son muy simples. Tanto que solo pueden hacer algo muy sencillo: cambiar ligeramente la estructura de las proteínas sanas para que pasen de ser solubles a insolubles.
Puede parecer algo irrelevante, pero lo cierto es que este cambio es catastrófico para el sistema nervioso. Estas proteínas zombi, al hacerse insolubles, no pueden diluirse en el interior de las células, por lo que empiezan a acumularse. Además, las enzimas degradadoras, conscientes de que aquello es una amenaza para el cuerpo, intentan degradarlas, pero no pueden, pues estos priones son resistentes a las proteasas, que son las enzimas que degradan proteínas.
A medida que la epidemia zombi se va expandiendo por el sistema nervioso, cada vez hay más y más priones. Llega un momento (generalmente mucho tiempo después de la infección) en el que ya no quedan prácticamente proteínas sanas (PrPc), sino las zombis, es decir, los priones (PrPSc). Es en este momento cuando la neurotransmisión no ocurre con normalidad que surgen los síntomas de las enfermedades priónicas.
Como es imposible reconvertir las proteínas zombi en las sanas, la muerte es inevitable. Esto explica que una de sus enfermedades (la famosa “enfermedad de las vacas locas”) sea la única patología del mundo con un 100% de letalidad.
¿Cómo se contagian los priones?
Llevamos todo el artículo hablando de que los priones son patógenos, pero ahora ha llegado el momento de hacer una puntualización. Y es que es cierto que provocan daños graves en el sistema nervioso, cosa propia de los gérmenes, pero no siempre hay un proceso infectivo. En otras palabras, el prión no siempre viene de fuera. Hay veces que “nace” en nuestro cuerpo.
Y es que una enfermedad priónica surge cuando un prión en nuestro organismo empieza a alterar la estructura de una proteína de nuestro cuerpo, lo que lleva a desarrollar daños lentos pero continuos en nuestro sistema nervioso central. Pero hay veces en las que este prión surge cuando hay algún defecto en nuestros genes (hereditario o no) que hace que, cuando las moléculas que traducen los genes en proteínas lean esa información errónea, generen el prión. Es nuestro propio cuerpo el que, por error, “crea” una proteína zombi que irá alterando la funcionalidad de las sanas.
En este sentido, dependiendo de cómo sea la aparición del prión, podemos hablar de enfermedades priónicas esporádicas (sin un componente hereditario y sin causa conocida, el gen de la proteína PrPc da lugar al prión), familiares (hay un componente hereditario a través del cual heredamos una mutación en el gen y desarrollamos el prión) o contraídas (el prión nos infecta por contacto con un tejido o material contaminado por la proteína zombi).
Las 5 enfermedades priónicas más importantes
Las enfermedades por priones son muy raras. De hecho, al año se diagnostica únicamente un caso por cada millón de habitantes. Y la mayoría de veces se desarrollan por causas genéticas (esporádicas o familiares), por lo que infectarse por un prión es algo enormemente improbable. Sea como sea, veamos las enfermedades causadas por priones más importantes.
1. Enfermedad de Creutzfeldt-Jakob
La única enfermedad del mundo con un 100% de letalidad. No hay tratamiento posible y la muerte ocurre inevitablemente entre 4 meses y 2 años después del inicio de la enfermedad (la esperanza de vida media es de 6 meses). El mecanismo de daño en el sistema nervioso es el mismo que hemos comentado anteriormente. De hecho, todas las enfermedades priónicas que veremos a continuación siguen el mismo.
En el caso de la enfermedad de Creutzfeldt-Jakob, la patología puede desarrollarse de distintas maneras. La forma más común es la esporádica, en la que por una causa desconocida se generan los priones en nuestro propio organismo. Es la responsable del 85% de casos de la enfermedad y suele desarrollarse a partir de los 60 años.
La siguiente forma más común es la familiar, en la que hay una herencia del gen mutado, por lo que la enfermedad suele desarrollarse a una edad más temprana. La neurodegeneración es más lenta y es responsable de entre el 5% y el 15% de los casos.
La forma menos común (es prácticamente imposible desarrollarla) pero la más famosa es la contraída, pues es aquella en la que hay una “infección” por parte de un prión, es decir, es un prión del exterior el que nos hace desarrollar la enfermedad. Esta aparece por comer carne de bovino contaminada con el prión (el mediático caso de “la enfermedad de las vacas locas”) o por pasar por intervenciones quirúrgicas en las que se utilizan herramientas contaminadas con la proteína zombi. De todos modos, en toda la historia solo se han registrado 230 casos en todo el mundo en los que la enfermedad se ha contraído desde fuera.
- Te recomendamos leer: “Las 10 enfermedades más letales en la actualidad”
2. Kuru
El kuru es una enfermedad priónica que se contagia por comer tejidos cerebrales de una persona que sufre la enfermedad de Creutzfeldt-Jakob. No hace falta decir, pues, lo extraña que es. De hecho, los únicos casos que se han reportado han sido en tribus de Papúa Nueva Guinea en las que hacían rituales de canibalismo como muestra de respeto para los familiares fallecidos. En lo que llevamos de siglo apenas se han diagnosticado 10 casos.
3. Insomnio mortal
El insomnio mortal es una enfermedad priónica que recibe este nombre porque la neurodegeneración da sus primeros síntomas con una fuerte alteración del sueño, aunque termina provocando la muerte a los 7 meses - 6 años de los primeros signos clínicos. Esta enfermedad puede desarrollarse de forma esporádica o familiar, pero nunca contraída.
4. Prionopatía variable sensible a proteasas
La prionopatía variable sensible a proteasas es una patología priónica que provoca alteraciones en el estado de ánimo y en la conducta de la persona, aunque termina por provocar la muerte aproximadamente dos años después de los primeros síntomas. Es responsable del 3% de las enfermedades priónicas y su incidencia es extremadamente baja: 1 caso por cada 100 millones de habitantes. Solo se presenta de forma esporádica y no se ha encontrado ninguna mutación que explique su aparición.
5. Enfermedad de Gerstmann-Sträussler-Scheinker
La enfermedad de Gerstmann-Sträussler-Scheinker es una enfermedad similar a la de Creutzfeldt-Jakob en sintomatología, aunque en este caso es mucho menos frecuente (y la de Creutzfeldt-Jakob ya era rara), solo tiene forma familiar (por herencia de una mutación), progresa de forma mucho más lenta (normalmente la muerte se produce a los 5 años) y se desarrolla a una edad más temprana (la de Creutzfeldt-Jakob lo hacía normalmente a los 60, pero esta a los 40). En este caso, la muerte suele producirse a causa de una neumonía, que surge por los problemas respiratorios vinculados al deterioro mental.